Minden ember élete során találkozik testekkel, amelyek a három halmazállapotú anyag valamelyikében vannak. A legegyszerűbben tanulmányozható aggregációs állapot a gáz. A cikkben megvizsgáljuk az ideális gáz fogalmát, megadjuk a rendszer állapotegyenletét, és figyelmet fordítunk az abszolút hőmérséklet leírására is.
Az anyag halmazállapota
Minden tanulónak jó ötlete van arról, hogy milyen halmazállapotról beszél, amikor meghallja a „gáz” szót. Ezt a szót olyan testként kell érteni, amely képes elfoglalni bármely számára biztosított térfogatot. Nem tudja megtartani formáját, mert a legkisebb külső hatásnak sem tud ellenállni. Ezenkívül a gáz nem tartja meg a térfogatát, ami nemcsak a szilárd anyagoktól, hanem a folyadékoktól is megkülönbözteti.
A folyadékokhoz hasonlóan a gáz is folyékony anyag. A szilárd testek gázokban történő mozgása során ez utóbbiak akadályozzák ezt a mozgást. A keletkező erőt ellenállásnak nevezzük. Értéke attól függa test sebessége a gázban.
Erős példák a gázokra a levegő, az otthonok fűtésére és főzéshez használt földgáz, a reklám izzócsövek kitöltésére használt közömbös gázok (Ne, Ar), vagy inert (nem agresszív, védő) környezet létrehozására hegesztés közben.
Ideális gáz
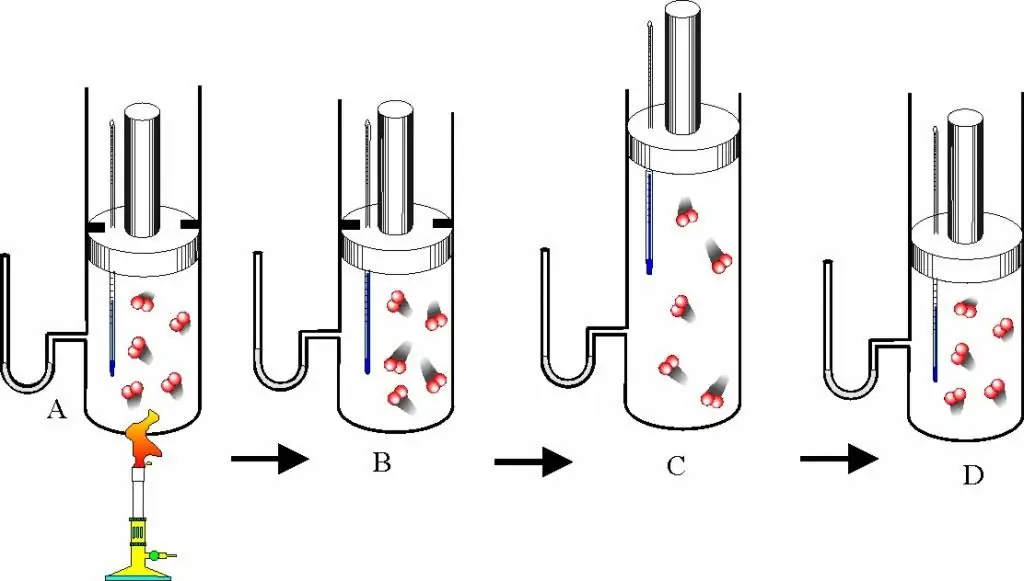
Mielőtt a gáztörvények és az állapotegyenlet leírásához kezdene, jól meg kell értenie azt a kérdést, hogy mi az ideális gáz. Ezt a koncepciót a molekuláris kinetikai elmélet (MKT) vezeti be. Ideális gáz minden olyan gáz, amely megfelel a következő jellemzőknek:
- Az ezt alkotó részecskék nem lépnek kölcsönhatásba egymással, kivéve a közvetlen mechanikai ütközéseket.
- A részecskéknek az edény falával vagy egymással való ütközésének eredményeként mozgási energiájuk és lendületük megmarad, vagyis az ütközést abszolút rugalmasnak tekintjük.
- A részecskéknek nincsenek méretei, de véges tömegük van, vagyis hasonlóak az anyagi pontokhoz.
Természetes, hogy minden gáz nem ideális, hanem valódi. Ennek ellenére számos gyakorlati probléma megoldásához ezek a közelítések teljesen helytállóak és használhatók. Létezik egy általános empirikus szabály, amely azt mondja: ha egy gáz kémiai természetétől függetlenül szobahőmérséklet feletti hőmérsékletű és légköri nagyságrendű vagy annál alacsonyabb nyomású, akkor nagy pontossággal ideálisnak tekinthető, és leírható vele. azt.az ideális gáz állapotegyenletének képlete.
Clapeyron-Mengyelejev törvény
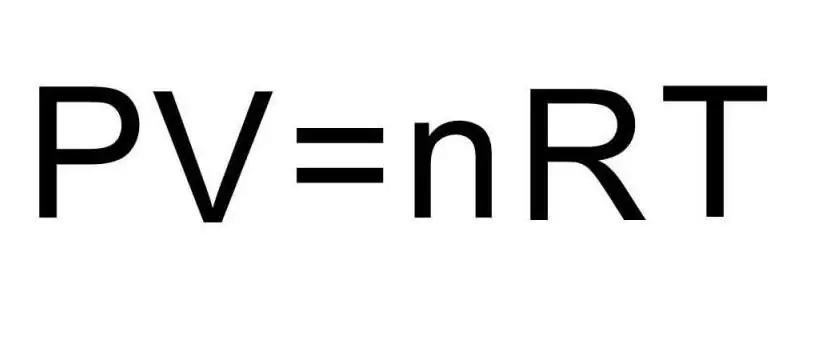
Az anyagok különböző halmazállapotai közötti átmeneteket és egyetlen halmazállapoton belüli folyamatokat a termodinamika kezeli. A nyomás, a hőmérséklet és a térfogat három olyan mennyiség, amelyek egyértelműen meghatározzák a termodinamikai rendszer bármely állapotát. Az ideális gáz állapotegyenletének képlete ezt a három mennyiséget egyetlen egyenlőséggé egyesíti. Írjuk fel ezt a képletet:
PV=nRT
Itt P, V, T - nyomás, térfogat, hőmérséklet, ill. Az n értéke az anyag mennyisége mólokban, az R szimbólum pedig a gázok univerzális állandóját jelöli. Ez az egyenlőség azt mutatja, hogy minél nagyobb a nyomás és a térfogat szorzata, annál nagyobbnak kell lennie az anyag mennyiségének és a hőmérsékletnek a szorzatának.

A gáz állapotegyenletének képletét Clapeyron-Mengyelejev törvénynek nevezik. 1834-ben Emile Clapeyron francia tudós elődei kísérleti eredményeit összegezve jutott ehhez az egyenlethez. Clapeyron azonban számos állandót használt, amelyeket Mengyelejev később eggyel helyettesített - az R univerzális gázállandóval (8, 314 J / (molK)). Ezért a modern fizikában ezt az egyenletet francia és orosz tudósok nevéről nevezték el.

Egyéb egyenletformák
Fentebb felírtuk a Mengyelejev-Clapeyron állapotegyenletet ideális gázra az általánosan elfogadott ill.kényelmes forma. A termodinamikai problémákban azonban gyakran egy kissé eltérő formára lehet szükség. Az alábbiakban további három képlet található, amelyek közvetlenül következnek az írott egyenletből:
PV=NkBT;
PV=m/MRT;
P=ρRT/M.
Ez a három egyenlet egy ideális gázra is univerzális, csak bennük jelennek meg olyan mennyiségek, mint m tömeg, M moláris tömeg, ρ sűrűség és a rendszert alkotó N részecskék száma. A kB szimbólum itt a Boltzmann-állandót jelöli (1, 3810-23J/K).
Boyle-Mariotte törvény
Amikor Clapeyron összeállította az egyenletét, olyan gáztörvényeken alapult, amelyeket több évtizeddel korábban kísérletileg fedeztek fel. Az egyik ilyen a Boyle-Mariotte törvény. Zárt rendszerben zajló izoterm folyamatot tükröz, melynek eredményeként olyan makroszkopikus paraméterek változnak, mint a nyomás és a térfogat. Ha egy ideális gáz állapotegyenletébe T és n állandót teszünk, akkor a gáztörvény a következő alakot veszi fel:
P1V1=P2V 2
Ez a Boyle-Mariotte törvény, amely szerint a nyomás és a térfogat szorzata megmarad egy tetszőleges izoterm folyamat során. Ebben az esetben maguk a P és V értékek megváltoznak.
Ha P(V) vagy V(P) ábrázolja, akkor az izotermák hiperbolák lesznek.
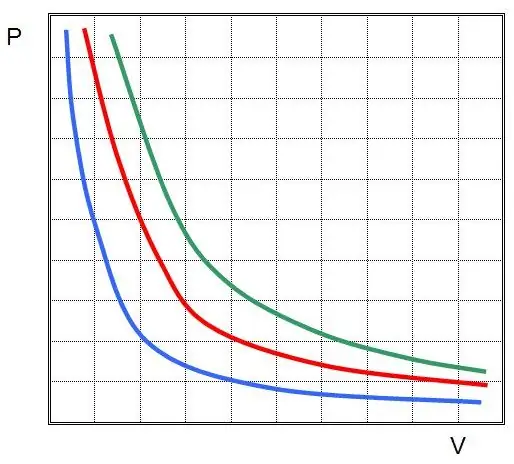
Charles és Gay-Lussac törvényei
Ezek a törvények matematikailag írják le az izobárt és az izokhorikusságotfolyamatok, vagyis olyan átmenetek a gázrendszer állapotai között, amelyekben a nyomás, illetve a térfogat megmarad. Károly törvénye matematikailag a következőképpen írható fel:
V/T=állandó, ha n, P=állandó
Gay-Lussac törvénye a következő:
P/T=állandó, ha n, V=állandó.
Ha mindkét egyenlőséget gráf formájában ábrázoljuk, akkor olyan egyeneseket kapunk, amelyek bizonyos szöget zárnak be az x tengelyhez képest. Az ilyen típusú grafikonok egyenes arányosságot mutatnak a térfogat és a hőmérséklet között állandó nyomáson, valamint a nyomás és a hőmérséklet között állandó térfogat mellett.
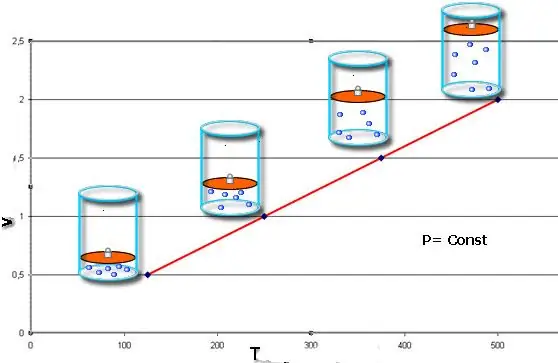
Ne feledje, hogy mindhárom figyelembe vett gáztörvény nem veszi figyelembe a gáz kémiai összetételét, valamint az anyagmennyiség változását.
Abszolút hőmérséklet
A mindennapi életben megszoktuk a Celsius-hőmérséklet-skálát, mivel ez alkalmas a körülöttünk zajló folyamatok leírására. Tehát a víz 100 oC-on forr, és 0 oC-on lefagy. A fizikában ez a skála kényelmetlennek bizonyul, ezért az úgynevezett abszolút hőmérsékleti skálát használják, amelyet Lord Kelvin vezetett be a 19. század közepén. Ennek a skálának megfelelően a hőmérsékletet Kelvinben (K) mérik.
Úgy tartják, -273, 15 oC hőmérsékleten az atomok és molekulák hőrezgései nincsenek, előrefelé irányuló mozgásuk teljesen leáll. Ez a hőmérséklet Celsius-fokban az abszolút nullának felel meg Kelvinben (0 K). Ebből a meghatározásbólaz abszolút hőmérséklet fizikai jelentése a következő: az anyagot alkotó részecskék, például atomok vagy molekulák kinetikus energiájának mértéke.
Az abszolút hőmérséklet fenti fizikai jelentése mellett más megközelítések is léteznek ennek a mennyiségnek a megértésére. Az egyik az említett Károly gáztörvény. Írjuk a következő formában:
V1/T1=V2/T 2=>
V1/V2=T1/T 2.
Az utolsó egyenlőség azt mondja, hogy a rendszerben lévő anyag bizonyos mennyiségénél (például 1 mol) és bizonyos nyomásnál (például 1 Pa) a gáz térfogata egyértelműen meghatározza az abszolút hőmérsékletet. Más szóval, a gáztérfogat növekedése ilyen körülmények között csak a hőmérséklet emelkedése miatt lehetséges, és a térfogat csökkenése a T értékének csökkenését jelzi.
Ne feledje, hogy a Celsius-hőmérséklettől eltérően az abszolút hőmérséklet nem lehet negatív.
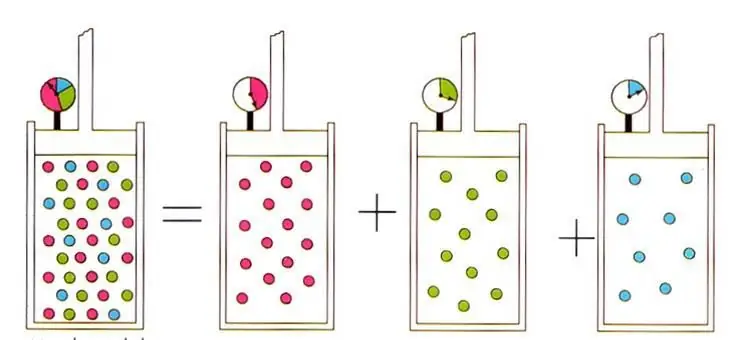
Avogadro-elv és gázkeverékek
A fenti gáztörvények mellett az ideális gáz állapotegyenlete is elvezet ahhoz az elvhez, amelyet Amedeo Avogadro fedezett fel a 19. század elején, amely a vezetéknevét viseli. Ez az elv megállapítja, hogy bármely gáz térfogatát állandó nyomáson és hőmérsékleten a rendszerben lévő anyag mennyisége határozza meg. A megfelelő képlet így néz ki:
n/V=állandó, ha P, T=állandó.
Az írott kifejezés az ideális gázfizikában jól ismert D alton-törvényhez vezet a gázkeverékekre. Eza törvény kimondja, hogy egy keverékben lévő gáz parciális nyomását egyértelműen annak atomfrakciója határozza meg.
Példa problémamegoldásra
Egy ideális gázt tartalmazó, merev falú zárt edényben a melegítés hatására a nyomás 3-szorosára nőtt. Meg kell határozni a rendszer végső hőmérsékletét, ha annak kezdeti értéke 25 oC.
Először is váltsuk át a hőmérsékletet Celsius-fokról Kelvinre, a következőket kapjuk:
T=25 + 273, 15=298, 15 K.
Mivel az edény falai merevek, a melegítési folyamat izokhorikusnak tekinthető. Erre az esetre a Meleg-Lussac törvényt alkalmazzuk, a következőkkel rendelkezünk:
P1/T1=P2/T 2=>
T2=P2/P1T 1.
Így a végső hőmérsékletet a nyomásviszony és a kezdeti hőmérséklet szorzatából határozzuk meg. Az adatokat egyenlőségre behelyettesítve a következő választ kapjuk: T2=894,45 K. Ez a hőmérséklet 621,3 oC.






