A minket körülvevő természeti jelenségek és folyamatok meglehetősen összetettek. Pontos fizikai leírásukhoz nehézkes matematikai apparátust kell használni, és számos jelentős tényezőt kell figyelembe venni. A probléma elkerülése érdekében a fizikában néhány egyszerűsített modellt használnak, amelyek nagyban megkönnyítik a folyamat matematikai elemzését, de gyakorlatilag nem befolyásolják a leírás pontosságát. Az egyik az ideális gázmodell. Vizsgáljuk meg részletesebben a cikkben.
Az ideális gáz fogalma
Az ideális gáz egy anyag aggregált állapota, amely olyan anyagi pontokból áll, amelyek nem lépnek kölcsönhatásba egymással. Magyarázzuk meg ezt a meghatározást részletesebben.
Először is, az anyagi pontokról, mint tárgyakról beszélünk, amelyek ideális gázt alkotnak. Ez azt jelenti, hogy molekuláinak és atomjainak nincs mérete, de bizonyos tömegük van. Ez merészegy közelítés tehető annak figyelembevételével, hogy minden valódi gázban alacsony nyomáson és magas hőmérsékleten a molekulák közötti távolság sokkal nagyobb, mint lineáris méreteik.
Másodszor, az ideális gázban lévő molekulák nem léphetnek kölcsönhatásba egymással. A valóságban ilyen interakciók mindig léteznek. Tehát még a nemesgázok atomjai is dipól-dipól vonzást tapasztalnak. Más szóval, van der Waals kölcsönhatások jelen vannak. A molekulák forgási és transzlációs mozgásának kinetikus energiájához képest azonban ezek a kölcsönhatások olyan kicsik, hogy nem befolyásolják a gázok tulajdonságait. Ezért ezeket nem lehet figyelembe venni a gyakorlati problémák megoldása során.
Fontos megjegyezni, hogy nem minden olyan gáz tekinthető ideálisnak, amelynek sűrűsége alacsony és hőmérséklete magas. A van der Waals kölcsönhatások mellett léteznek más, erősebb típusú kötések is, például a H2O molekulák közötti hidrogénkötések, amelyek a gázidealitási feltételek durva megsértéséhez vezetnek. Emiatt a vízgőz nem ideális gáz, a levegő viszont az.
Egy ideális gáz fizikai modellje
Ez a modell a következőképpen ábrázolható: tegyük fel, hogy a gázrendszer N részecskét tartalmaz. Ezek különböző vegyi anyagok és elemek atomjai és molekulái lehetnek. Az N részecskék száma nagy, ezért leírására általában a "mol" mértékegységet használják (1 mól Avogadro számának felel meg). Mindegyik valamilyen térfogatban mozog V. Részecskemozgásokkaotikusak és függetlenek egymástól. Mindegyiknek van egy bizonyos v sebessége, és egyenes úton halad.
Elméletileg a részecskék ütközésének valószínűsége majdnem nulla, mivel méretük kicsi a részecskék közötti távolságokhoz képest. Ha azonban ilyen ütközés történik, akkor az abszolút rugalmas. Ez utóbbi esetben a részecskék összimpulzusa és mozgási energiája megmarad.
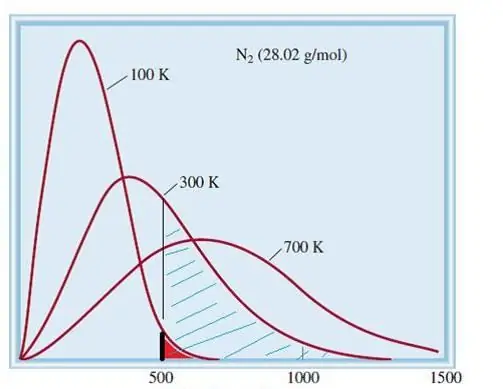
Az ideális gázok figyelembe vett modellje egy klasszikus rendszer, rengeteg elemmel. Ezért a benne lévő részecskék sebessége és energiája Maxwell-Boltzmann statisztikai eloszlásának engedelmeskedik. Egyes részecskék sebessége alacsony, míg mások nagy sebességgel rendelkeznek. Ebben az esetben van egy bizonyos szűk sebességhatár, amelyben ennek a mennyiségnek a legvalószínűbb értékei rejlenek. A nitrogénmolekulák sebességeloszlását az alábbiakban mutatjuk be sematikusan.
Gázok kinetikai elmélete
Az ideális gázok fent leírt modellje egyedileg határozza meg a gázok tulajdonságait. Ezt a modellt először Daniel Bernoulli javasolta 1738-ban.

Ezt követően August Kroenig, Rudolf Clausius, Mihail Lomonoszov, James Maxwell, Ludwig Boltzmann, Marian Smoluchowski és más tudósok fejlesztették ki jelenlegi állapotáig.
A folyékony anyagok kinetikai elmélete, amelyre az ideális gázmodell épül, a rendszer két fontos makroszkopikus tulajdonságát magyarázza meg mikroszkópikus viselkedése alapján:
- A gázok nyomása a részecskéknek az edény falával való ütközésének eredménye.
- A rendszer hőmérséklete a molekulák és atomok állandó mozgásának megnyilvánulásának eredménye.
Bővítsük ki a kinetikai elmélet mindkét következtetését.
Gáznyomás
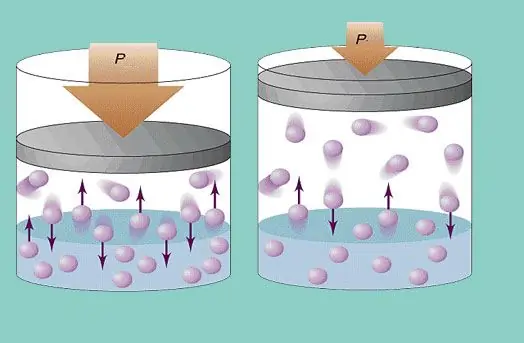
Az ideális gázmodell a részecskék állandó kaotikus mozgását feltételezi a rendszerben, és állandó ütközést az edény falával. Minden ilyen ütközés abszolút rugalmasnak tekinthető. A részecske tömege kicsi (≈10-27-10-25 kg). Ezért nem tud nagy nyomást létrehozni ütközéskor. Ennek ellenére a részecskék száma, és így az ütközések száma is óriási (≈1023). Ezenkívül az elemek négyzetes középsebessége szobahőmérsékleten több száz méter másodpercenként. Mindez az edény falán érezhető nyomás kialakulásához vezet. A következő képlettel számítható ki:
P=Nmvcp2 / (3V), ahol vcp a négyzetes középsebesség, m a részecske tömege.
Abszolút hőmérséklet
Az ideális gázmodell szerint a hőmérsékletet egyedileg a vizsgált rendszerben lévő molekula vagy atom átlagos kinetikus energiája határozza meg. Felírhatja a következő kifejezést, amely egy ideális gáz kinetikus energiájához és abszolút hőmérsékletéhez kapcsolódik:
mvcp2 / 2=3/2kB T.
Itt kB a Boltzmann-állandó. Ebből az egyenlőségből a következőt kapjuk:
T=m vcp2 / (3kB).
Univerzális állapotegyenlet
Ha a fenti kifejezéseket kombináljuk P abszolút nyomásra és T abszolút hőmérsékletre, akkor a következő egyenlőséget írhatjuk fel:
PV=nRT.
Itt n az anyag mennyisége mólokban, R a D. I. Mengyelejev által bevezetett gázállandó. Ez a kifejezés az ideális gázok elméletének legfontosabb egyenlete, mivel három termodinamikai paramétert (V, P, T) egyesít, és nem függ a gázrendszer kémiai jellemzőitől.

Az univerzális egyenletet először Emile Clapeyron francia fizikus vezette le kísérletileg a 19. században, majd Mengyelejev orosz kémikus hozta modern formájává, ezért viseli jelenleg ezeknek a tudósoknak a nevét.






