A világ, amelyben élünk, elképzelhetetlenül szép, és tele van számos különféle folyamattal, amelyek meghatározzák az élet menetét. Mindezeket a folyamatokat az ismert tudomány - a fizika - tanulmányozza. Lehetőséget ad arra, hogy legalább némi képet kapjunk az univerzum eredetéről. Ebben a cikkben egy olyan fogalmat fogunk megvizsgálni, mint a molekuláris kinetikai elmélet, egyenletei, típusai és képletei. Mielőtt azonban rátérne e kérdések mélyebb tanulmányozására, tisztáznia kell magának a fizika jelentését és az általa vizsgált területeket.
Mi a fizika?

Valójában ez egy nagyon kiterjedt tudomány, és talán az egyik legalapvetőbb az emberiség történetében. Például, ha ugyanaz a számítástechnika az emberi tevékenység szinte minden területéhez kapcsolódik, legyen szó számítógépes tervezésről vagy rajzfilmek készítéséről, akkor a fizika maga az élet, annak összetett folyamatainak és folyamatainak leírása. Próbáljuk meg kitalálni a jelentését, amennyire csak lehet, egyszerűsítve a megértést.
SzóvalA fizika tehát olyan tudomány, amely az energia és az anyag, a köztük lévő összefüggések tanulmányozásával, a hatalmas univerzumunkban előforduló számos folyamat magyarázatával foglalkozik. Az anyag szerkezetének molekuláris-kinetikai elmélete csak egy kis csepp az elméletek és a fizika ágai tengerében.
Az energia, amelyet ez a tudomány részletesen tanulmányoz, sokféle formában ábrázolható. Például fény, mozgás, gravitáció, sugárzás, elektromosság és sok más formában. Ebben a cikkben ezen formák szerkezetének molekuláris kinetikai elméletét fogjuk érinteni.
Az anyag tanulmányozása képet ad az anyag atomi szerkezetéről. Egyébként a molekuláris-kinetikai elméletből következik. Az anyag szerkezetének tudománya lehetővé teszi számunkra, hogy megértsük és megtaláljuk létezésünk értelmét, az élet és magának az Univerzumnak az okait. Még mindig próbáljuk meg tanulmányozni az anyag molekuláris kinetikai elméletét.
Először is, némi bevezetésre van szükség a terminológia és a következtetések teljes megértéséhez.
Fizikai témák
Arra a kérdésre válaszolva, hogy mi a molekuláris-kinetikai elmélet, nem lehet nem beszélni a fizika szakaszairól. Ezek mindegyike az emberi élet egy adott területének részletes tanulmányozásával és magyarázatával foglalkozik. Besorolásuk a következő:
- Mechanika, amely további két részre oszlik: kinematika és dinamika.
- Statikus.
- Termodinamika.
- Molekuláris metszet.
- Elektrodinamika.
- Optika.
- A kvantumok és az atommag fizikája.
Beszéljünk konkrétan a molekulárisrólfizika, mert a molekuláris-kinetikai elméleten alapul.
Mi a termodinamika?
Általában a molekuláris rész és a termodinamika a fizika szorosan összefüggő ágai, amelyek kizárólag az összes fizikai rendszer makroszkopikus összetevőjét vizsgálják. Érdemes megjegyezni, hogy ezek a tudományok pontosan leírják a testek és anyagok belső állapotát. Például állapotuk hevítés, kristályosodás, párolgás és kondenzáció során, atomi szinten. Más szóval, a molekuláris fizika olyan rendszerek tudománya, amelyek hatalmas számú részecskéből állnak: atomokból és molekulákból.
Ezek a tudományok tanulmányozták a molekuláris kinetikai elmélet főbb rendelkezéseit.
Már a hetedik évfolyamon megismerkedtünk a mikro- és makrovilágok, rendszerek fogalmaival. Nem lesz felesleges frissíteni ezeket a kifejezéseket a memóriában.
A mikrovilág, ahogy a nevéből is láthatjuk, elemi részecskékből áll. Más szóval, ez a kis részecskék világa. Méretük a 10-18 m és 10-4 m közötti tartományban van mérve, és tényleges állapotuk ideje elérheti a végtelent és a aránytalanul kis időközök, például 10-20 s.
A makrovilág stabil formájú testeket és rendszereket tekint, amelyek sok elemi részecskéből állnak. Az ilyen rendszerek arányosak emberi méretünkkel.
Emellett van olyan, hogy megavilág. Hatalmas bolygókból, kozmikus galaxisokból és komplexumokból áll.
Alapokelmélet
Most, hogy egy kicsit összefogl altuk, és emlékeztünk a fizika alapvető fogalmaira, egyenesen a cikk fő témájához térhetünk.
A molekuláris-kinetikai elmélet a tizenkilencedik században jelent meg és fogalmazták meg először. Lényege abban rejlik, hogy részletesen leírja bármely anyag szerkezetét (gyakrabban a gázok szerkezetét, mint a szilárd és folyékony testeket), három alapvető rendelkezés alapján, amelyeket olyan kiemelkedő tudósok feltételezéseiből gyűjtöttek össze, mint Robert Hooke, Isaac. Newton, Daniel Bernoulli, Mihail Lomonoszov és még sokan mások.
A molekuláris kinetikai elmélet főbb rendelkezései így hangzanak:
- Abszolút minden anyag (függetlenül attól, hogy folyékony, szilárd vagy gáz halmazállapotú) összetett szerkezetű, kisebb részecskékből áll: molekulákból és atomokból. Az atomokat néha "elemi molekuláknak" nevezik.
- Ezek az elemi részecskék mindig folyamatos és kaotikus mozgásban vannak. Mindannyian találkoztunk ennek a tételnek a közvetlen bizonyítékával, de valószínűleg nem tulajdonítottunk neki nagy jelentőséget. Például mindannyian láttuk a napsugarak hátterében, hogy a porszemcsék folyamatosan kaotikus irányba mozognak. Ez annak köszönhető, hogy az atomok kölcsönös lökéseket hajtanak végre egymással, folyamatosan kinetikus energiát adva egymásnak. Ezt a jelenséget először 1827-ben tanulmányozták, és a felfedezőről nevezték el - "Brown-mozgás".
- Minden elemi részecske folyamatos kölcsönhatásban van egymássalbizonyos erők, amelyeknek elektromos kőzetük van.
Érdemes megjegyezni, hogy egy másik példa, amely leírja a kettes számú pozíciót, és amely például a gázok molekuláris kinetikai elméletére is vonatkozhat, a diffúzió. Találkozunk vele a mindennapi életben, valamint számos tesztnél és ellenőrzésnél, ezért fontos, hogy legyen róla elképzelésünk.
Először is nézze meg a következő példákat:
Az orvos véletlenül alkoholt öntött ki egy lombikból az asztalra. Vagy talán leejtette a parfümös üvegét, és az egész földre terült.
Miért ebben a két esetben az alkohol és a parfüm illata egy idő után az egész helyiséget betölti, és nem csak azt a területet, ahol ezeknek az anyagoknak a tartalma kiömlött?
A válasz egyszerű: diffúzió.
Diffúzió - mi ez? Hogyan folyik?

Ez egy olyan folyamat, amelyben az egyik anyagot alkotó részecskék (általában gáz) behatolnak egy másik anyag intermolekuláris üregeibe. A fenti példáinkban a következő történt: a termikus, azaz folyamatos és disszociált mozgás következtében alkohol és/vagy parfüm molekulák kerültek a levegőmolekulák közötti résbe. Fokozatosan, az atomokkal és a levegő molekuláival való ütközés hatására szétterjednek a helyiségben. A diffúzió intenzitása, vagyis áramlásának sebessége egyébként a diffúzióban részt vevő anyagok sűrűségétől, valamint atomjaik és molekuláik mozgási energiájától, az úgynevezett kinetikustól függ. Minél nagyobb a kinetikus energia, annál nagyobb ezeknek a molekuláknak a sebessége és az intenzitása.
A leggyorsabb diffúziós folyamatot nevezhetjük diffúziónak a gázokban. Ennek oka az a tény, hogy a gáz összetételében nem homogén, ami azt jelenti, hogy a gázokban lévő intermolekuláris üregek jelentős mennyiségű helyet foglalnak el, és az idegen anyag atomjainak és molekuláinak bejuttatása könnyebben és gyorsabban megy végbe..
Ez a folyamat egy kicsit lassabb folyadékokban. A kockacukor feloldódása egy bögre teában csak egy példa a szilárd anyag folyadékban való diffúziójára.
De a leghosszabb idő a diffúzió a szilárd kristályszerkezetű testekben. Ez pontosan így van, mert a szilárd anyagok szerkezete homogén, erős kristályrácsos, melynek sejtjeiben a szilárd anyag atomjai rezegnek. Például, ha két fémrúd felületét jól megtisztítjuk, majd érintkezésbe hozzuk egymással, akkor kellően hosszú idő elteltével képesek leszünk felismerni az egyik fém darabjait a másikban, és fordítva.
Mint minden más alapvető részhez hasonlóan a fizika alapelmélete is külön részekre oszlik: osztályozás, típusok, képletek, egyenletek stb. Így megtanultuk a molekuláris kinetikai elmélet alapjait. Ez azt jelenti, hogy nyugodtan folytathatja az egyes elméleti blokkok mérlegelését.
Gázok molekuláris-kinetikai elmélete
Meg kell érteni a gázelmélet rendelkezéseit. Mint korábban említettük, figyelembe vesszük a gázok makroszkopikus jellemzőit, például a nyomást és a hőmérsékletet. EzKésőbb szükség lesz a gázok molekuláris-kinetikai elméletének egyenletének levezetéséhez. De a matematika - később, és most foglalkozzunk az elmélettel és ennek megfelelően a fizikával.
A tudósok megfogalmazták a gázok molekuláris elméletének öt rendelkezését, amelyek a gázok kinetikai modelljének megértését szolgálják. Így hangzanak:
- Minden gáz elemi részecskékből áll, amelyeknek nincs meghatározott mérete, de tömegük van. Más szóval, ezeknek a részecskéknek a térfogata minimális a köztük lévő hosszhoz képest.
- A gázok atomjainak és molekuláinak gyakorlatilag nincs potenciális energiájuk, illetve a törvény szerint minden energia egyenlő a kinetikaival.
- Ezzel az állásponttal már korábban is megismerkedtünk - Brown-mozdulat. Vagyis a gázrészecskék mindig folyamatos és kaotikus mozgásban vannak.
- A gázrészecskék minden kölcsönös ütközése, amelyet a sebesség és az energia üzenete kísér, teljesen rugalmas. Ez azt jelenti, hogy az ütközés során nincs energiaveszteség vagy éles ugrás a mozgási energiájukban.
- Normál körülmények között és állandó hőmérsékleten a részecskék mozgásának átlagos energiája szinte minden gáz esetében azonos.
Átírhatjuk az ötödik pozíciót a gázok molekuláris-kinetikai elméletének ilyen típusú egyenletével:
E=1/2mv^2=3/2kT, ahol k a Boltzmann-állandó; T - hőmérséklet Kelvinben.
Ez az egyenlet lehetővé teszi számunkra, hogy megértsük a gáz elemi részecskéinek sebessége és abszolút hőmérsékletük közötti összefüggést. Ennek megfelelően minél magasabb az abszolútértékükannál nagyobb a sebességük és a mozgási energiájuk.
Gáznyomás
A karakterisztika ilyen makroszkopikus összetevői, mint például a gázok nyomása, szintén megmagyarázhatók a kinetikai elmélettel. Ehhez képzeljük el a következő példát.
Tegyük fel, hogy valamilyen gáz molekulája van egy dobozban, amelynek hossza L. Használjuk a gázelmélet fentebb leírt rendelkezéseit, és vegyük figyelembe, hogy a molekulagömb csak az x mentén mozog -tengely. Így megfigyelhetjük majd az edény (doboz) egyik falával való rugalmas ütközés folyamatát.
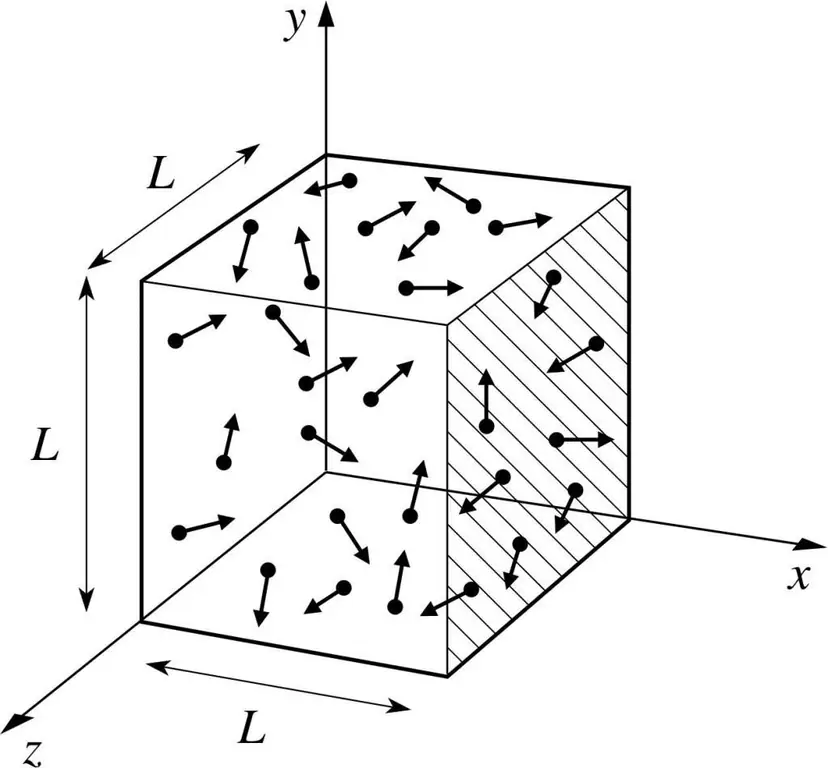
A folyamatban lévő ütközés lendületét, mint tudjuk, a következő képlet határozza meg: p=mv, de ebben az esetben ez a képlet vetületi formát vesz fel: p=mv(x).
Mivel csak az x tengely, azaz az x tengely méretét vesszük figyelembe, a lendület teljes változását a következő képlet fejezi ki: mv(x) - m(-v(x))=2mv(x).
Ezután vegyük figyelembe a tárgyunk által kifejtett erőt Newton második törvénye alapján: F=ma=P/t.
Ezekből a képletekből fejezzük ki a gázoldali nyomást: P=F/a;
Most cseréljük be az erőkifejezést a kapott képletbe, és kapjuk: P=mv(x)^2/L^3.
Ezek után a kész nyomásképletünket az N-edik gázmolekulára írhatjuk fel. Más szavakkal, így fog kinézni:
P=Nmv(x)^2/V, ahol v a sebesség és V a hangerő.
Most próbáljunk meg néhány alapvető rendelkezést kiemelni a gáznyomással kapcsolatban:
- Ezen keresztül nyilvánul megmolekulák ütközése annak az objektumnak a falának molekuláival, amelyben az található.
- A nyomás nagysága egyenesen arányos a molekuláknak az edény falára gyakorolt hatásának erejével és sebességével.
Néhány rövid következtetés az elméletről
Mielőtt továbbmennénk és megvizsgálnánk a molekuláris kinetikai elmélet alapegyenletét, néhány rövid következtetést ajánlunk a fenti pontokból és elméletből:
- Atomjai és molekulái átlagos mozgási energiájának mértéke az abszolút hőmérséklet.
- Ha két különböző gáz azonos hőmérsékletű, molekuláik átlagos kinetikus energiája azonos.
- A gázrészecskék energiája egyenesen arányos az átlagos négyzetsebességgel: E=1/2mv^2.
- Bár a gázmolekulák átlagos kinetikus energiával és átlagos sebességgel rendelkeznek, az egyes részecskék különböző sebességgel mozognak: egyesek gyorsan, mások lassan.
- Minél magasabb a hőmérséklet, annál nagyobb a molekulák sebessége.
- Hányszor növeljük a gáz hőmérsékletét (például duplájára), részecskéinek mozgási energiája annyiszorosára (illetve kétszeresére) nő.
Alapegyenlet és képletek

A molekuláris kinetikai elmélet alapegyenlete lehetővé teszi a mikrovilág mennyiségei és ennek megfelelően a makroszkopikus, azaz mért mennyiségek közötti kapcsolat megállapítását.
Az egyik legegyszerűbb modell, amelyet a molekuláris elmélet figyelembe vehet, az ideális gázmodell.
Mondhatnádez egyfajta képzeletbeli modell, amelyet az ideális gáz molekuláris kinetikai elmélete tanulmányoz, amelyben:
- a legegyszerűbb gázrészecskéket tökéletesen rugalmas golyóknak tekintjük, amelyek csak egyetlen esetben lépnek kölcsönhatásba egymással és bármely edény falának molekuláival - ez abszolút rugalmas ütközés;
- a gázon belüli vonzási erők hiányoznak, vagy valójában elhanyagolhatók;
- a gáz belső szerkezetének elemei anyagi pontnak vehetők, azaz térfogatuk is elhanyagolható.
Egy modell figyelembevételével Rudolf Clausius német származású fizikus megírta a gáznyomás képletét a mikro- és makroszkopikus paraméterek kapcsolatán keresztül. Így néz ki:
p=1/3m(0)nv^2.
Később ezt a képletet az ideális gáz molekuláris-kinetikai elméletének alapegyenletének nevezik. Többféle formában is bemutatható. Most az a feladatunk, hogy olyan szakaszokat mutassunk be, mint a molekuláris fizika, a molekuláris kinetikai elmélet, és így ezek teljes egyenletei és típusai. Ezért érdemes az alapképlet más változatait is figyelembe venni.
Tudjuk, hogy a gázmolekulák mozgását jellemző átlagos energia a következő képlettel kereshető: E=m(0)v^2/2.
Ebben az esetben az eredeti nyomásképletben szereplő m(0)v^2 kifejezést helyettesíthetjük az átlagos mozgási energiával. Ennek eredményeként lehetőségünk lesz a gázok molekuláris kinetikai elméletének alapegyenletének összeállítására a következő formában: p=2/3nE.
Emellett mindannyian tudjuk, hogy az m(0)n kifejezés két hányados szorzataként írható fel:
m/NN/V=m/V=ρ.
Ezen manipulációk után átírhatjuk az ideális gáz molekuláris-kinetikai elméletének egyenletére vonatkozó képletünket egy harmadik, eltérő formában:
p=1/3ρv^2.
Nos, talán csak ennyit kell tudni erről a témáról. Már csak a megszerzett ismereteket kell rendszerezni rövid (és nem olyan) következtetések formájában.
Minden általános következtetés és képlet a "Molekuláris-kinetikai elmélet" témában
Kezdjük hát.
Először:
A fizika a természettudományok körébe tartozó alaptudomány, amely az anyag és az energia tulajdonságait, szerkezetét, a szervetlen természet mintázatait vizsgálja.
A következő szakaszokat tartalmazza:
- mechanika (kinematika és dinamika);
- statikus;
- termodinamika;
- elektrodinamika;
- molekuláris szakasz;
- optika;
- a kvantumok és az atommag fizikája.
Második:
A részecskefizika és a termodinamika szorosan összefüggő ágak, amelyek a fizikai rendszerek teljes számának kizárólag makroszkopikus összetevőit vizsgálják, vagyis a rengeteg elemi részecskéből álló rendszereket.
Molekuláris kinetikai elméleten alapulnak.
Harmadik:
A dolog lényege ez. A molekuláris kinetikai elmélet részletesen leírja egy anyag szerkezetét (gyakrabban a gázok, mint a szilárd anyagok szerkezetét).és folyékony testek) három alapvető feltevésen alapul, amelyeket kiemelkedő tudósok feltételezéseiből gyűjtöttek össze. Köztük: Robert Hooke, Isaac Newton, Daniel Bernoulli, Mihail Lomonoszov és még sokan mások.
Negyedik:
A molekuláris kinetikai elmélet három alaptétele:
- Minden anyag (függetlenül attól, hogy folyékony, szilárd vagy gázhalmazállapotú) összetett szerkezetű, amely kisebb részecskékből áll: molekulákból és atomokból.
- Ezek az egyszerű részecskék folyamatos kaotikus mozgásban vannak. Példa: Brown-mozgás és diffúzió.
- Minden molekula bármilyen körülmények között kölcsönhatásba lép egymással bizonyos erőkkel, amelyeknek elektromos kőzetük van.
A molekuláris kinetikai elmélet ezen rendelkezéseinek mindegyike szilárd alapot jelent az anyag szerkezetének tanulmányozásában.
Ötödik:
A gázmodell molekuláris elméletének több fő pontja:
- Minden gáz elemi részecskékből áll, amelyeknek nincs meghatározott mérete, de tömegük van. Más szavakkal, ezeknek a részecskéknek a térfogata minimális a köztük lévő távolságokhoz képest.
- A gázok atomjainak és molekuláinak gyakorlatilag nincs potenciális energiájuk, összenergiájuk megegyezik a kinetikus energiával.
- Ezzel az állásponttal már korábban is megismerkedtünk - Brown-mozdulat. Vagyis a gázrészecskék mindig folyamatos és véletlenszerű mozgásban vannak.
- Abszolút minden atomok és gázmolekulák kölcsönös ütközése, amelyhez a sebesség és az energia üzenete társul, teljesen rugalmas. Ezazt jelenti, hogy az ütközés során nincs energiaveszteség vagy éles ugrás a mozgási energiájukban.
- Normál körülmények és állandó hőmérséklet mellett szinte minden gáz átlagos mozgási energiája azonos.
Hatodik:
Következtetések a gázokra vonatkozó elméletből:
- Az abszolút hőmérséklet az atomok és molekulák átlagos kinetikus energiájának mértéke.
- Ha két különböző gáz azonos hőmérsékletű, molekuláik átlagos kinetikus energiája azonos.
- A gázrészecskék átlagos kinetikus energiája egyenesen arányos a négyzetes középsebességgel: E=1/2mv^2.
- Bár a gázmolekulák átlagos kinetikus energiával és átlagos sebességgel rendelkeznek, az egyes részecskék különböző sebességgel mozognak: egyesek gyorsan, mások lassan.
- Minél magasabb a hőmérséklet, annál nagyobb a molekulák sebessége.
- Hányszor növeljük a gáz hőmérsékletét (például duplájára), részecskéinek átlagos mozgási energiája is ennyiszeresére (illetve megkétszereződik) nő.
- A gáznak az edény falára gyakorolt nyomása és a molekulák e falakra gyakorolt hatásának intenzitása közötti kapcsolat egyenesen arányos: minél több az ütközés, annál nagyobb a nyomás, és fordítva..
Hetedik:
Az ideális gázmodell olyan modell, amelyben a következő feltételeknek kell teljesülniük:
- A gázmolekulák tökéletesen rugalmas golyóknak tekinthetők, és azok is.
- Ezek a golyók kölcsönhatásba léphetnek egymással és bármelyik falávalhajó csak egy esetben - abszolút rugalmas ütközés.
- Azok az erők, amelyek leírják a gáz atomjai és molekulái közötti kölcsönös tolóerőt, hiányoznak vagy elhanyagolhatók.
- Az atomokat és molekulákat anyagi pontoknak tekintjük, vagyis a térfogatuk is elhanyagolható.
Nyolcadik:
Adjuk meg az összes alapegyenletet és mutassuk meg a képleteket a "Molekuláris-kinetikai elmélet" témakörben:
p=1/3m(0)nv^2 - az ideális gázmodell alapegyenlete, amelyet Rudolf Clausius német fizikus állított le.
p=2/3nE - az ideális gáz molekuláris-kinetikai elméletének alapegyenlete. A molekulák átlagos kinetikus energiájából származik.
р=1/3ρv^2 - ugyanaz az egyenlet, de az ideális gázmolekulák sűrűségén és négyzetes középsebességén keresztül vizsgáljuk.
m(0)=M/N(a) - a képlet egy molekula tömegének az Avogadro-számon keresztül történő meghatározásához.
v^2=(v(1)+v(2)+v(3)+…)/N - képlet a molekulák átlagos négyzetes sebességének meghatározásához, ahol v(1), v(2), v (3) és így tovább - az első molekula, a második, a harmadik és így tovább az n-edik molekula sebessége.
n=N/V - képlet a molekulák koncentrációjának meghatározásához, ahol N a molekulák száma egy adott V térfogatú gáztérfogatban.
E=mv^2/2=3/2kT - képletek a molekulák átlagos kinetikus energiájának meghatározásához, ahol v^2 a molekulák négyzetes középsebessége, k egy állandó az osztrák Ludwig Boltzmann fizikájáról elnevezett érték, T pedig a gáz hőmérséklete.
p=nkT - nyomásképlet a koncentrációban, állandóBoltzmann és az abszolút hőmérséklet T. Ebből egy másik alapvető képlet következik, amelyet Mengyelejev orosz tudós és Claiperon francia fizikus-mérnök fedezett fel:
pV=m/MRT, ahol R=kN(a) a gázok univerzális állandója.
Most mutassuk meg a különböző izofolyamatok állandóit: izobár, izokhorikus, izoterm és adiabatikus.
pV/T=const - akkor hajtják végre, ha a gáz tömege és összetétele állandó.
рV=állandó - ha a hőmérséklet is állandó.
V/T=állandó - ha a gáznyomás állandó.
p/T=const - ha a hangerő állandó.
Talán csak ennyit kell tudni erről a témáról.
Ma egy olyan tudományterületbe csöppentünk bele, mint az elméleti fizika, annak több szakasza és blokkja. Részletesebben érintettük a fizika egy olyan területét, mint az alapvető molekuláris fizika és a termodinamika, nevezetesen a molekuláris-kinetikai elméletet, amely a kezdeti vizsgálat során úgy tűnik, nem okoz nehézséget, de valójában számos buktatója van.. Kibővíti az ideális gázmodellről alkotott ismereteinket, amelyet szintén részletesen tanulmányoztunk. Emellett érdemes megjegyezni, hogy megismerkedtünk a molekulaelmélet alapegyenleteivel is azok változatos változataiban, és átgondoltuk az összes legszükségesebb képletet bizonyos ismeretlen mennyiségek megtalálásához ebben a témában, ez különösen az írásra való felkészülés során lesz hasznos. bármilyen tesztet, vizsgát és tesztet, vagy a fizika általános szemléletének és ismereteinek bővítése érdekében.
Reméljük, hogy ez a cikk hasznos volt az Ön számára, és csak a legszükségesebb információkat gyűjtötte ki belőle, megerősítve tudását a termodinamika olyan pilléreiben, mint a molekuláris kinetikai elmélet alapvető rendelkezései.






