A mi korunkban a fizika nagyon elterjedt tudomány lett. Szó szerint mindenhol jelen van. A legelemibb példa: egy almafa nő az udvaron, és érnek rajta a gyümölcsök, eljön az idő és hullani kezdenek az almák, de milyen irányba hullanak? Az univerzális gravitáció törvényének köszönhetően magzatunk a földre esik, vagyis lemegy, de fel nem. A fizika egyik leghíresebb példája volt, de figyeljünk a termodinamikára, pontosabban a fázisegyensúlyokra, amelyek nem kevésbé fontosak az életünkben.
Termodinamika

Először is nézzük meg ezt a kifejezést. ΘερΜοδυναΜική - így néz ki a szó görögül. Az első rész ΘερΜo „meleget”, a második δυναΜική pedig „erőt” jelent. A termodinamika a fizika egyik ága, amely a makroszkopikus rendszerek tulajdonságait, valamint az energia átalakításának és átvitelének különféle módjait tanulmányozza. Ebben a részben speciálisan különböző állapotokat és folyamatokat tanulmányozunk, hogy a hőmérséklet fogalmát be lehessen vinni a leírásba (ez egy termodinamikai rendszert jellemző fizikai mennyiség, amelynek mérésebizonyos készülékek). A termodinamikai rendszerekben zajló összes folyamatot csak mikroszkopikus mennyiségek írják le (nyomás és hőmérséklet, valamint az összetevők koncentrációja).
Clapeyron-Clausius egyenlet
Minden fizikus ismeri ezt az egyenletet, de bontsuk szét darabonként. Bizonyos anyagok egyik fázisból a másikba való átmenetének egyensúlyi folyamataira utal. Ez jól látható az ilyen példákon: olvasztás, párolgás, szublimáció (a termékek tartósításának egyik módja, amely a nedvesség teljes eltávolításával megy végbe). A képlet egyértelműen mutatja a folyamatban lévő folyamatokat:
- n=PV/RT;
- ahol T az anyag hőmérséklete;
- P-nyomás;
- R-fajlagos fázisátalakulási hő;
- V-módosítás adott hangerőben.
Az egyenlet keletkezésének története

A Clausius-Clapeyron egyenlet kiváló matematikai magyarázata a termodinamika második főtételének. „Clausius-egyenlőtlenségnek” is nevezik. A tételt természetesen maga a tudós dolgozta ki, aki meg akarta magyarázni a rendszerben lévő hőáramlás és az entrópia, valamint a környezet kapcsolatát. Ezt az egyenletet Clausius dolgozta ki, amikor megpróbálta megmagyarázni és számszerűsíteni az entrópiát. Szó szerinti értelemben a tétel lehetőséget ad annak meghatározására, hogy egy ciklikus folyamat reverzibilis vagy irreverzibilis. Ez az egyenlőtlenség kvantitatív képletet kínál a második törvény megértéséhez.
A tudós az elsők között dolgozott az entrópia gondolatán, és még fel is adta.folyamat neve. A ma Clausius-tételként emlegetett tételt először 1862-ben publikálták Rudolf hatodik művében, A transzformációs ekvivalencia tétel felhasználásáról belső munkában. A tudós megpróbált arányos kapcsolatot kimutatni az entrópia és az energiaáramlás között fűtéssel (δ Q) a rendszerben. Az építőiparban ez a hőenergia munkává, ciklikus folyamattal pedig hővé alakítható. Rudolph bebizonyította, hogy "a ciklikus folyamatban előforduló összes transzformáció algebrai összege csak nullánál lehet kisebb, vagy szélsőséges esetben egyenlő nullával."
Zárt elszigetelt rendszer
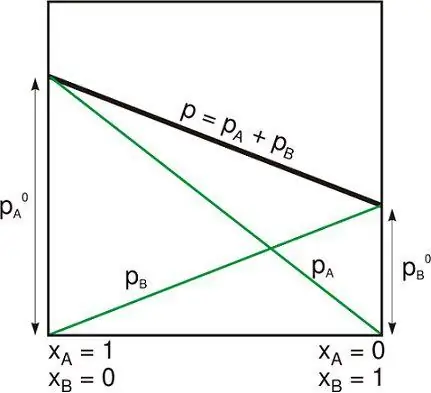
Az izolált rendszer a következők egyike:
- A fizikai rendszer távol áll azoktól, amelyek nem lépnek kapcsolatba velük.
- A termodinamikai rendszert merev, mozdíthatatlan falak zárják le, amelyeken sem anyag, sem energia nem tud áthaladni.
Annak ellenére, hogy az alany belső viszonyban áll saját gravitációjával, egy elszigetelt rendszert általában túllépnek a külső gravitációs és egyéb távoli erők határain.
Ez szembeállítható azzal, amit (a termodinamikában használt általánosabb terminológiával) zárt rendszernek neveznek, amelyet szelektív falak vesznek körül, amelyen keresztül az energia hő vagy munka formájában továbbítható, de nem anyag. És egy nyitott rendszerrel, amelyben az anyag és az energia belép vagy kilép, bár különféle áthatolhatatlan falai lehetnek bennehatárainak részei.
Egy elszigetelt rendszer betartja a természetvédelmi törvényt. A termodinamikában leggyakrabban az anyagot és az energiát külön fogalomnak tekintik.
Termodinamikai átmenetek
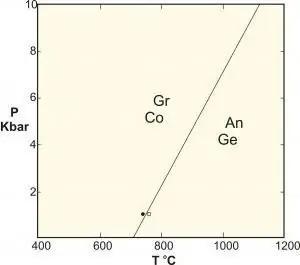
A kvantum fázisátalakulások megértéséhez hasznos összehasonlítani őket a klasszikus transzformációkkal (más néven termikus inverziókkal). A CPT leírja a rendszer termodinamikai tulajdonságainak csúcsát. A részecskék átrendeződését jelzi. Tipikus példa a víz fagyásos átmenete, amely a folyadék és a szilárd anyag közötti sima átmenetet írja le. A klasszikus fázisnövekedés a rendszer energiája és a hőingadozások entrópiája közötti versengésnek köszönhető.
Egy klasszikus rendszernek nulla hőmérsékleten nincs entrópiája, ezért nem fordulhat elő fázisátalakulás. Ezek sorrendjét az első nem folytonos derivált termodinamikai potenciál határozza meg. És természetesen megvan az első sorrend. A ferromágnesről paramágnesre történő fázisátalakítás folyamatos és másodrendű. Ezeket az állandó változásokat a rendezett fázisból a rendezetlen fázisba egy sorrendi paraméter írja le, amely nulla. A fenti ferromágneses transzformációnál a rendelési paraméter a rendszer teljes mágnesezettsége lesz.
Gibbs-potenciál
A Gibbs Free Energy az a maximális munkamennyiség tágulás nélkül, amely eltávolítható egy termodinamikus zárt rendszerből (amely képes hőcserélni és együttműködni a környezettel). Ilyena maximális eredményt csak teljesen reverzibilis folyamatban lehet elérni. Amikor a rendszer visszaváltozik az első állapotból a másodikba, a Gibbs-szabadenergia csökkenése megegyezik a rendszer által a környezetében végrehajtott csökkenéssel, mínusz a nyomóerők munkája.
Egyenlegállapotok

A termodinamikai és mechanikai egyensúly a termodinamika axiomatikus fogalma. Ez egy vagy több rendszer belső állapota, amelyeket többé-kevésbé áteresztő vagy át nem eresztő falak kötnek össze. Ebben az állapotban nincsenek tiszta makroszkopikus anyag- vagy energiaáramlások sem egy rendszeren belül, sem a rendszerek között.
A belső egyensúlyi állapot saját felfogása szerint makroszkopikus változás nem következik be. A rendszerek egyszerre vannak kölcsönös termikus, mechanikai, kémiai (állandó), sugárzási egyensúlyban. Lehetnek ugyanabban a formában. Ebben a folyamatban az összes nézet egyszerre és korlátlan ideig mentésre kerül, amíg a fizikai művelet meg nem szakad. Makroszkópikus egyensúlyban tökéletesen precíz kiegyensúlyozott cserék mennek végbe. A fenti bizonyíték ennek a fogalomnak a fizikai magyarázata.
Alapok
Minden törvénynek, tételnek, képletnek megvan a maga alapja. Nézzük meg a fázisegyensúly törvényének 3 alapját.
- A fázis az anyag egy formája, kémiai összetételében, fizikai állapotában és mechanikai egyensúlyában homogén. A tipikus fázisok szilárd, folyékony és gázhalmazállapotúak. Két nem elegyedő folyadékot (vagy különböző összetételű folyékony keveréket), amelyeket külön határvonal választ el, két különálló fázisnak és nem elegyedő szilárd anyagnak tekintjük.
- A komponensek száma (C) a rendszer kémiailag független komponenseinek száma. A független fajok minimális száma a rendszer összes fázisának összetételének meghatározásához.
- A szabadsági fokok száma (F) ebben az összefüggésben az egymástól független intenzív változók száma.
Osztályozás fázisegyensúlyok szerint
- Folyamatos nettó átviteli reakciók (gyakran szilárd fázisú reakcióknak nevezik) különböző összetételű szilárd anyagok között mennek végbe. Tartalmazhatnak folyadékokban található elemeket (H, C), de ezek az elemek szilárd fázisban megmaradnak, így folyékony fázisok nem vesznek részt reagensként vagy termékként (H2O, CO2). A szilárd, tiszta átviteli reakciók lehetnek folyamatosak vagy nem folytonosak, vagy terminálisak.
- A polimorf a szilárd fázisú reakció egy speciális típusa, amely azonos összetételű fázisokat tartalmaz. Klasszikus példák erre az alumínium-szilikátok, kianit-szilmanit-andaluzit reakciók, a grafit nagy nyomáson történő gyémánttá történő átalakulása és a kalcium-karbonát egyensúlya.
Egyensúlyi törvények

A Gibbs-gyári szabályt Josiah Willard Gibbs javasolta a "The Equilibrium of Heterogeneous Substances" című híres tanulmányában, amely 1875 és 1878 között jelent meg. Arra vonatkoziknem-reaktív többkomponensű heterogén rendszerek termodinamikai egyensúlyban, és egy adott egyenlőség:
- F=C-P+2;
- ahol F a szabadsági fokok száma;
- C - alkatrészek száma;
- P - egymással termodinamikai egyensúlyban lévő fázisok száma.
A szabadsági fokok száma a nem fogl alt intenzív változók száma. A legnagyobb számú termodinamikai paraméter, mint például a hőmérséklet vagy a nyomás, amelyek egyidejűleg és tetszőlegesen változhatnak anélkül, hogy egymást befolyásolnák. Az egykomponensű rendszerre példa az egyetlen tiszta vegyszert tartalmazó rendszer, míg a kétkomponensű rendszerek, például a víz és etanol keverékei, két független komponensből állnak. A tipikus fázisátalakulások (fázisegyensúly) a szilárd anyagok, folyadékok, gázok.
Fázisszabály állandó nyomáson
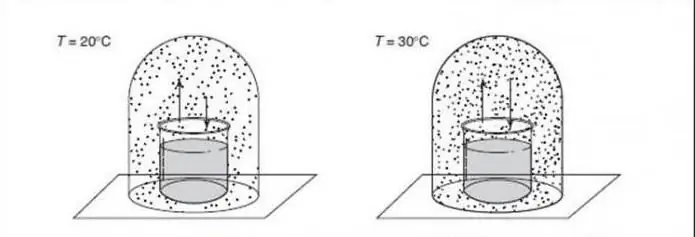
A különböző szilárd szerkezetek közötti fázisváltozásokkal foglalkozó anyagtudományi alkalmazásoknál gyakran fordul elő állandó nyomás (pl. egy atmoszféra), amelyet szabadsági fokként figyelmen kívül hagynak, így a szabály a következő lesz: F=C - P + 1.
Ezt a képletet néha "sűrített fázisszabály" néven vezetik be, de mint tudjuk, nem alkalmazható ezekre a nagy nyomásnak kitett rendszerekre (például a geológiában), mivel ezek következményei a nyomás katasztrofális következményekkel járhat.
Úgy tűnhet, hogy a fázisegyensúly csak egy üres kifejezés, és kevés olyan fizikai folyamat van, amelyben ez a pillanatrészt vesz, de, mint láttuk, enélkül sok általunk ismert törvény nem működik, ezért meg kell ismerkedni ezekkel az egyedi, színes, bár kissé unalmas szabályokkal. Ez a tudás sok embernek segített. Megtanulták, hogyan alkalmazzák ezeket önmagukra, például a villanyszerelők, ismerve a fázisokkal végzett munka szabályait, megvédhetik magukat a szükségtelen veszélyektől.

