Az ideális gáz tulajdonságainak tanulmányozása fontos téma a fizikában. A gázrendszerek jellemzőinek bemutatása a Boyle-Mariotte egyenlet figyelembevételével kezdődik, mivel ez az ideális gáz első kísérletileg felfedezett törvénye. Vizsgáljuk meg részletesebben a cikkben.
Mit jelent ideális gáz?
Mielőtt a Boyle-Mariotte törvényről és az azt leíró egyenletről beszélnénk, határozzuk meg az ideális gázt. Általában folyékony anyagként értik, amelyben az azt alkotó részecskék nem lépnek kölcsönhatásba egymással, és méretük elhanyagolhatóan kicsi az átlagos részecskék közötti távolságokhoz képest.
Valójában minden gáz valódi, vagyis az alkotó atomok és molekulák meghatározott méretűek, és nem lépnek kölcsönhatásba egymással van der Waals-erők segítségével. Magas abszolút hőmérsékleten (több mint 300 K) és alacsony nyomáson (egy atmoszféránál kevesebb) azonban az atomok és molekulák kinetikus energiája sokkal nagyobb, mint a van der Waals kölcsönhatások energiája, így a valódi gáz a jelzetta nagy pontosságú körülmények ideálisnak tekinthetők.
Boyle-Mariotte egyenlet
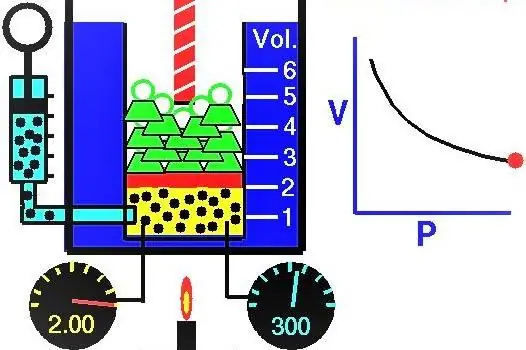
A gázok tulajdonságai Az európai tudósok aktívan kutakodtak a XVII-XIX. században. A legelső kísérleti úton felfedezett gáztörvény a gázrendszer tágulásának és összenyomódásának izoterm folyamatait leíró törvény volt. A megfelelő kísérleteket Robert Boyle 1662-ben és Edm Mariotte 1676-ban végezte. E tudósok mindegyike egymástól függetlenül kimutatta, hogy egy zárt gázrendszerben zajló izoterm folyamat során a nyomás a térfogattal fordítottan változik. A folyamat kísérletileg kapott matematikai kifejezését a következő formában írjuk le:
PV=k
Ahol P és V a rendszer nyomása és térfogata, ott k valamilyen állandó, amelynek értéke a gázanyag mennyiségétől és hőmérsékletétől függ. Ha a P(V) függvény függőségét egy gráfra építjük fel, akkor az hiperbola lesz. Az alábbiakban egy példa látható ezekre a görbékre.
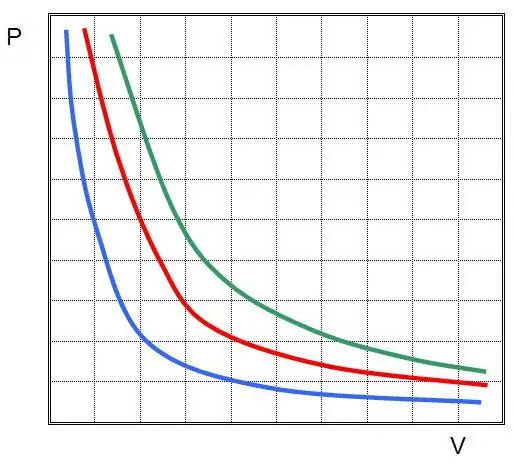
Az írott egyenlőséget Boyle-Mariotte egyenletnek (törvénynek) nevezik. Ez a törvény röviden a következőképpen fogalmazható meg: az ideális gáz állandó hőmérsékleten történő tágulása a benne lévő nyomás arányos csökkenéséhez vezet, éppen ellenkezőleg, a gázrendszer izoterm kompressziója a nyomás arányos növekedésével jár együtt.
Az ideális gázegyenlet
Boyle-Mariotte törvény egy speciális esete egy általánosabb törvénynek, amely Mengyelejev ésClapeyron. Emile Clapeyron, összefoglalva a gázok különféle külső körülmények közötti viselkedésére vonatkozó kísérleti információkat, 1834-ben a következő egyenletet kapta:
PV=nRT
Más szóval egy gázrendszer V térfogatának és a benne lévő P nyomásnak a szorzata egyenesen arányos a T abszolút hőmérséklet és az n anyag mennyiségének szorzatával. Ennek az arányosságnak az együtthatóját R betűvel jelöljük, és gáz univerzális állandónak nevezzük. Az írott egyenletben az R értéke számos konstans cseréje miatt jelent meg, amelyet Dmitrij Ivanovics Mengyelejev végzett 1874-ben.
Az egyetemes állapotegyenletből könnyen belátható, hogy a hőmérséklet és az anyagmennyiség állandósága garantálja az egyenlet jobb oldalának változatlanságát, ami azt jelenti, hogy az egyenlet bal oldala is állandó marad. Ebben az esetben a Boyle-Mariotte egyenletet kapjuk.

Egyéb gáztörvények
A fenti bekezdésben felírt Clapeyron-Mendeleev egyenlet három termodinamikai paramétert tartalmaz: P, V és T. Ha ezek mindegyike rögzített, és a másik kettő változhat, akkor a Boyle-Mariotte-t kapjuk, Charles és Gay-Lussac egyenletek. Charles törvénye a térfogat és a hőmérséklet egyenes arányosságáról beszél izobár folyamat esetén, a Gay-Lussac törvénye pedig azt, hogy izochor átmenet esetén a gáznyomás az abszolút hőmérséklettel egyenes arányban nő vagy csökken. A megfelelő egyenletek így néznek ki:
V/T=állandó, ha P=állandó;
P/T=állandó, amikor V=állandó.
SzóvalÍgy a Boyle-Mariotte-törvény a három fő gáztörvény egyike. Grafikus függőségében azonban eltér a többitől: a V(T) és P(T) függvények egyenesek, a P(V) függvények egy hiperbola.
Példa egy feladatra a Boyle-Mariotte törvény alkalmazásához
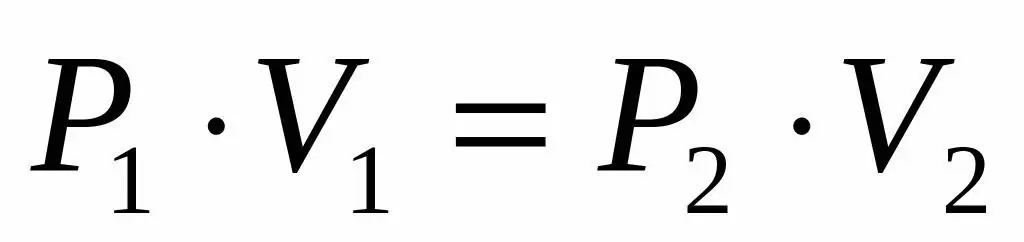
A kiindulási helyzetben a dugattyú alatti hengerben lévő gáz térfogata 2 liter, nyomása 1 atmoszféra volt. Mekkora volt a gáz nyomása, miután a dugattyú megemelkedett és a gázrendszer térfogata 0,5 literrel nőtt. A folyamat izotermnek számít.
Mivel adott egy ideális gáz nyomása és térfogata, és azt is tudjuk, hogy a hőmérséklet változatlan marad a tágulása során, a Boyle-Mariotte egyenletet a következő formában használhatjuk:
P1V1=P2V 2
Ez az egyenlőség azt mondja, hogy a térfogat-nyomás szorzat a gáz minden állapotára állandó egy adott hőmérsékleten. Az egyenlőségből a P2 értéket kifejezve megkapjuk a végső képletet:
P2=P1V1/V 2
A nyomásszámításnál ebben az esetben használhatunk rendszeren kívüli mértékegységeket, mert a literek zsugorodnak, és a nyomást P2atmoszférában kapjuk. A feltétel adatait behelyettesítve a probléma kérdésére a válaszhoz jutunk: P2=0,8 atmoszféra.






